以下文章来源于佰傲谷BioValley ,作者傲骨
2月8日,全国疫情地图实时报告显示,截止2月7日24时,全国新型冠状病毒感染的肺炎累积确诊病例31774人,累积死亡722人,危重患者救治成为疫情抗击工作的重点。
自疫情伊始,网上就开始流传各类新型冠状病毒“特效药”的说法。2月3日,国家卫健委发布《新型冠状病毒感染的肺炎诊疗方案(试行第五版)》。相比
起之前版本,第五版诊疗方案具有更强的指导性和可操作性,对重症患者的救治进行了优化。其中在新型冠状病毒导致的肺炎治疗方面,第五版诊疗方案首次明确:
“目前没有确认有效的抗病毒治疗方法”。这一提法也对各类网传“特效药”做出了一个明确判断,即这些药物目前并不是针对新型冠状病毒感染治疗的特效药物,
其疗效并未获得完全证明,必须在医生指导下谨慎使用,防止滥用。

事实上,由于新型冠状病毒疫情的出现,抗病毒药物再次获得了全社会的广泛关注。那么,近年来有哪些抗病毒新药获批上市,抗病毒药物研发领域又有哪些新的成果与进展?
已获批的抗病毒药物
表1、2009年至2019年FDA批准的抗病毒新药▽

十年来,FDA共批准了35款抗病毒药物,其中绝大部分针对的是由人免疫缺陷病毒、乙肝病毒、丙肝病毒和疱疹病毒所导致的慢性感染。而获批用于治疗
急性病毒感染的药物数量稀少,十年间仅有BioCryst
Pharmaceuticals的Rapivab与Genentech的Xofluza获批上市。
Rapivab是FDA批准的首款静脉注射用神经氨酸酶抑制剂,也是该类药物中第三个获批的产品。而Xofluza是首个口服单剂抗病毒药,也是
20年来首个具有创新作用机制的抗流感病毒药物。1月30日,罗氏药品部门主要负责人Bill
Anderson对路透社表示,Xofluza是为抗击季节性流感设计而成,不太可能对冠状病毒有效。
这也意味着,目前常见治疗急性病毒感染药物多为获批20年以上的“老药”。
表2、过去30年内获批的抗病毒急性感染药物▽

过去30年间,包括Rapivab和Xofluza在内,FDA共批准了5款抗病毒急性感染药物,且都为抗流感药物。根据2019年美国疾控中心流
感抗病毒药物治疗建议,仅推荐三款神经氨酸酶抑制剂Zanamivir、Oseltamivir、Peramivir和帽依赖性内切核酸酶抑制剂
Baloxavir Marboxil进行抗流感病毒治疗,金刚烷胺和金刚烷乙胺由于耐药性问题不再被推荐。
上述抗流感病毒药物中,Oseltamivir(国内称作奥司他韦)曾一度被报道用于治疗新型冠状病毒感染的肺炎患者。除了疫情初期流传于网络的武
汉协和医院诊疗方案中提到使用奥司他韦进行治疗外,1月24日,一篇发表于Lancet上题为“Clinical features of
patients infected with 2019 novel coronavirus in Wuhan,
China”的文章中提到,鉴于2019-nCov肺炎病例出现在流感高发期,疾病控制中经验性地采用了抗生素和奥司他韦的治疗。

1月26日,一篇发表于Science China:Life Science上题为“Evolution of the novel
coronavirus from the ongoing Wuhan outbreak and modeling of its spike
protein for risk of human
transmission”文章发现,新型冠状病毒致病机制与SARS类似,是通过病毒表面膜蛋白中的S蛋白与人ACE2受体结合进入宿主细胞,引起
ACE2表达下调,从而影响肾素-血管紧张素系统(RAS),而肺脏由于存在大量ACE2受体,因此成为SARS主攻点。


△新型冠状病毒S蛋白与ACE2结合的结构建模
而神经氨酸酶则是一种存在于流感病毒表面,可以协助成熟流感病毒脱离宿主细胞感染新的细胞,对流感病毒复制和扩散起关键作用的酶。有分析认为,由于流感病毒和SARS病毒致病机制上的不同,奥司他韦目前并没有明确证据显示其对SARS或新型冠状病毒有效。
此外,鉴于新型冠状病毒与SARS的相似性,无效结果也可以从一篇2004年发表在Emerging Infection
Diseases上题为“Inhibition of SARS Coronavirus Infection inVitro with
Clinically Approved Antiviral
Drugs”的文章中得到印证。研究中,新加坡团队对19款已上市抗病毒药物对SARS导致细胞病变的抑制效果进行了测试。结果显示,神经氨酸酶抑制剂奥
司他韦和扎那米韦对SARS无抑制效果。

不过该研究也给新型冠状病毒的药物筛选提供了一定参考。其中干扰素Wellferon(Interferonα-n1)、
Alferon(Interferonα-n3)、Betaferon(Interferon
β-1b)与核苷类似物Ribavirin(国内称作利巴韦林)都对SARS显示出抑制作用。而卫健委此次发布的新型冠状病毒诊疗方案中同样提到了α干扰
素吸入治疗和加用利巴韦林。
干扰素和利巴韦林虽然作用机制不同,但均为靶向宿主的抗病毒药物。过去30年间,FDA仅批准了13款靶向宿主,可发挥间接抗病毒作用的药物。
表3、FDA批准的靶向宿主抗病毒药物▽

干扰素是一种具有高度种属特异性的糖蛋白,可以通过诱导细胞合成抗病毒蛋白(AVP)发挥作用,并不能直接灭活病毒。具体而言,干扰素可以作用于细
胞干扰素受体,经过一系列信号传导等过程,激活细胞基因表达抗病毒蛋白,实现病毒的抑制。多种抗病毒蛋白可以阻断病毒mRNA与宿主细胞核糖体之间的相互
结合,抑制病毒多肽链合成效果,阻断病毒复制。此外干扰素还可以通过增强NK细胞和K细胞杀伤活性等效果,进行免疫调节。
核苷类似物是一种经修饰和改造的核苷类化合物,结构与天然核苷相似,可参与病毒代谢,却无法被病毒识别,干扰病毒基因表达,达到抗病毒作用。具体而
言,核苷类似物由细胞内激酶磷酸化后,可以通过在病毒进行基因复制时,掺入外源核苷酸导致复制终止。还可以与延伸的核苷酸链结合,导致天然核苷酸错配,引
发可损害RNA合成或影响蛋白表达的突变,最终导致病毒死亡。
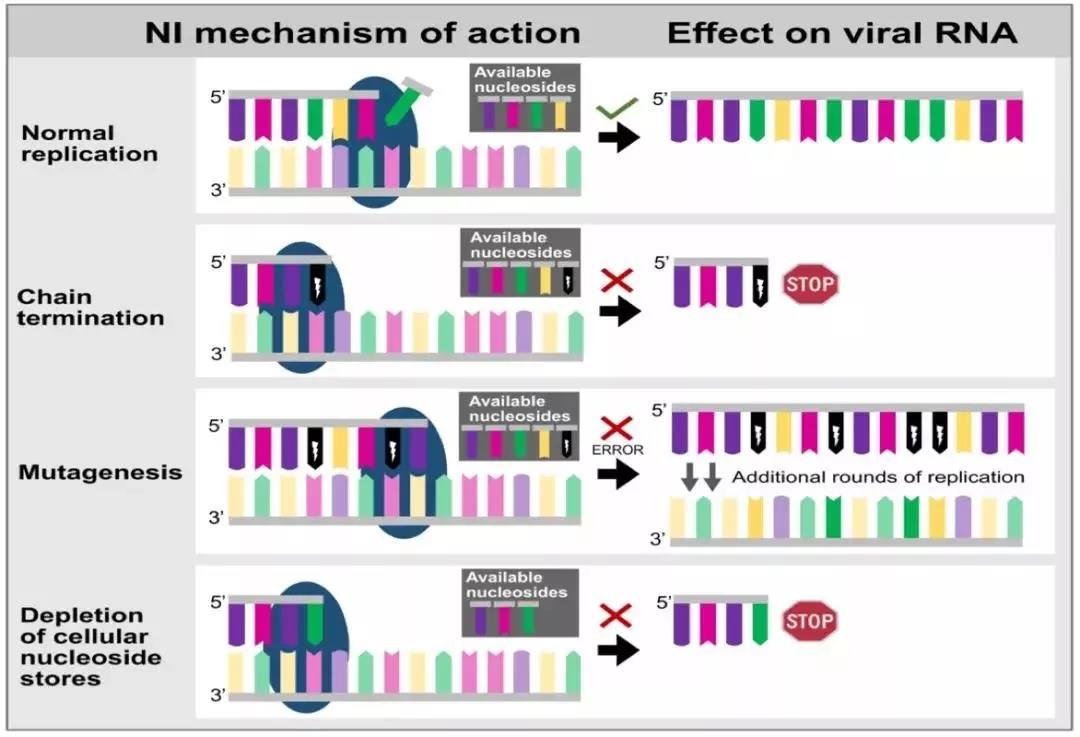
△核苷类似物作用原理
由于靶向宿主的作用机制,干扰素与核苷类似物都具有一定程度的广谱抗病毒特性,对多种慢性或急性病毒感染具有抑制作用,然而这种非特异性特点也伴随
着一些负面效果。例如干扰素进入人体后会刺激机体产生一系列内源性细胞因子。这些细胞因子作为特异性/非特异性免疫反应的介质,在人的神经、内分泌、免疫
调节中扮演重要角色。而这些细胞所导致的细胞程序反应可能会导致患者发热、头痛、关节酸痛、白细胞和血小板下降、精神及神经系统症状等。而核苷类似物,例
如利巴韦林则会通过细胞表面的ES-核苷载体无特异性进入包括红细胞在内所有类型细胞。而红细胞由于无法水解利巴韦林三磷酸盐,并且三磷酸盐也无法通过红
细胞膜,就会导致三磷酸盐在红细胞内富集,使红细胞膜受到氧化损伤、破裂,最终导致溶血性贫血。
“老药新用”是此次新型冠状病毒治疗的主要思路,除上文所提到的药物外,还有几款老药也获得了新的关注。
表4、两款被提到的蛋白酶抑制剂
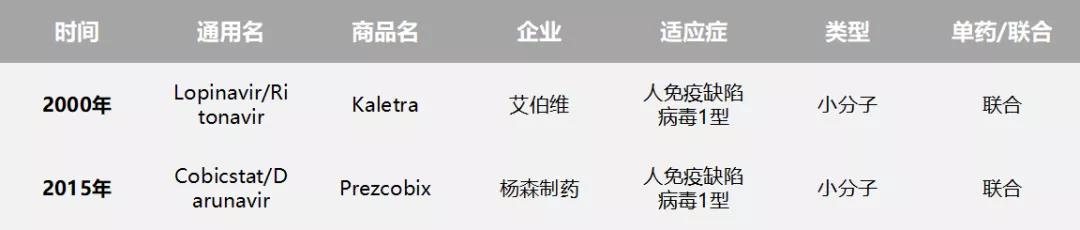
此次新型冠状病毒疫情中,蛋白酶抑制剂也多次出现在媒体报道中。1月23日,新型冠状病毒感染的肺炎专家组成员王广发接受采访时提到,一种名为“洛
匹那韦/利托那韦片”的药物,对他的个例来说有效。洛匹那韦/利托那韦于2000年获得美国FDA批准,商品名Kaletra,国内称作“克力芝”。

2月4日,国家卫健委表示正在收集“克力芝”和一些中药治疗的临床试验数据。同日,中国工程院院士、国家卫健委高级别专家组成员李兰娟团队公布新型
冠状病毒感染的肺炎的最新研究成果并提到“达芦那韦在300微摩尔浓度下,能显著抑制病毒复制,与未用药无处理组比较,抑制效率达280倍。”达芦那韦/
考比司他于2015年获得美国FDA批准,商品名Prezcobix,国内称作“普力泽”。这两款药物均属于蛋白酶抑制剂,最初获批用于人免疫缺陷病毒1
型的抗病毒治疗。
在体外研究中,HIV-1蛋白酶抑制剂被发现可以对冠状病毒主蛋白酶(3CLpro蛋白酶)产生抑制作用,而3CLpro蛋白酶在SARS病毒多聚
蛋白加工成功能蛋白和病毒成熟过程中发挥了关键作用。因此,包括“克力芝”、“普力泽”在内的蛋白酶抑制剂被看作为抗冠状病毒感染的潜在药物。
2017年9月,一篇线上发表于《Archives of Clinical Infectious
Diseases》题为“Lopinavir; A Potent Drug against Coronavirus Infection:
Insight from Molecular Docking
Study”文章通过软件模拟小分子与蛋白的相互作用和分子动力学试验,评估了HIV-1蛋白酶抑制剂对冠状病毒蛋白酶的影响。结果显示洛匹那韦和沙奎那
韦分别是冠状病毒蛋白酶的最强和最弱的抑制剂。

△根据小分子与蛋白相互作用和分子动力学试验得出的多维度数据,计算而得的多种蛋白酶抑制剂对SARS病毒的抑制能力。
李兰娟院士团队提出的另一款药物是阿比朵尔(Arbidol,Umifenovir)。该药物由前苏联药物化学研究中心研制开发,仅在俄罗斯与中国
获批上市用于治疗流感。阿比朵尔的作用机制一直被认为与血细胞凝集素酶相关。在流感病毒进入细胞形成吞噬体后,血细胞凝集素酶构象在pH变化下发生改变并
与细胞质膜融合,使病毒基因组进入宿主细胞开始复制。而阿比朵尔则可以增加血细胞凝集素酶构象的稳定性,抑制由血细胞凝集素所介导的膜融合,发挥抗病毒作
用。
抗病毒药物的研发进展
除了老药新用外,许多在研新药也进入了研究人员视野。而近期最为出名的要数吉利德研发的Remdesivir,国内称为瑞德西韦。
2月1号,一篇在线发表于《新英格兰医学杂志》上题为“First Case of 2019 Novel Coronavirus in the
United
States”文章在介绍美国首例确诊新型冠状病毒患者的诊疗过程中提到“医生决定为其提供一种尚未获批的药物——瑞德西韦”。2月3日,北京中日友好医
院宣布在武汉展开瑞德西韦随机、双盲、安慰剂对照III期临床试验,旨在确定瑞德西韦治疗新型冠状病毒的安全性和有效性。据新华社报道,2月5日,瑞德西
韦已经完成临床试验注册审批,2月6日首批新型冠状病毒感染的肺炎患者就将接受用药。

瑞德西韦是一种小分子核苷类似物,研发代号GS-5734。研究表明该药物对人畜共患冠状病毒有效,并能抑制人原代气管上皮细胞中SARS冠状病毒
和MERS冠状病毒的复制。其作用机制被认为是可以与RNA依赖的RNA聚合酶竞争底物,从而干扰病毒合成。RNA依赖的RNA聚合酶广泛存在于正链和双
链RNA病毒的RNA聚合酶,并发挥以单链RNA为模板合成互补RNA链的作用,在病毒基因组复制和转录中扮演了关键角色。而这一作用机制也使瑞德西韦具
有潜在的广谱抗病毒效果,包括此次新型冠状病毒。
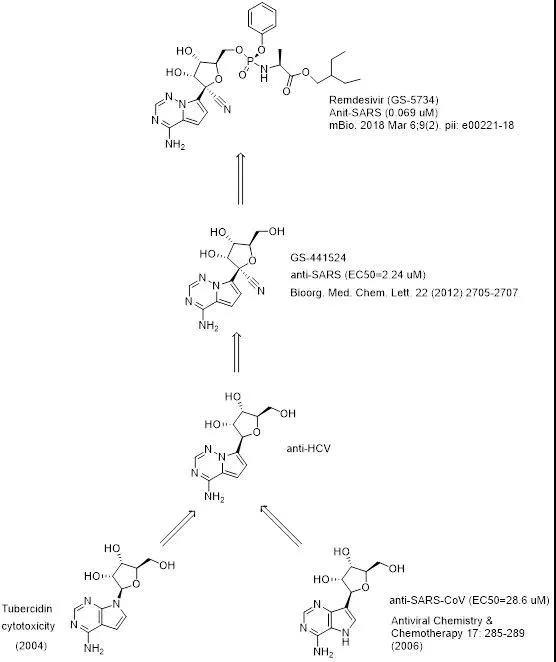
△吉利德报告的瑞德西韦优化过程
2月4日,一篇发表于《Nature》子刊 Cell Research上题为“Remdesivir and chloroquine
effectively inhibit the recently emerged novel coronavirus (2019-nCoV)
in vitro”的文章认为,体外实验显示,瑞德西韦可以有效控制新型冠状病毒感染。

△瑞德西韦对新型冠状病毒的体外抗病毒活性
除此之外,近年来快速发展的大分子抗体药物也成为抗病毒药物新的发展方向。2月3日,再生元宣布与美国卫生和公共服务部扩大合作,研发针对新型冠状
病毒的治疗性抗体药物。此前,再生元开发了一款代号为REGN-EB3的埃博拉治疗性抗体药物,该药物由三种抗体成分组成。在一项埃博拉病毒疗法随机对照
试验中显示出了最好的疗效,该实验于2019年12月发表于新英格兰医学杂志上。
根据ClinicalTrials,以“coronavirus”“2019-nCoVs”为关键词搜索正处于活跃状态(除去状态未知)的临床试验
共有21个,其中有关新型冠状病毒的临床试验就有12项。这些临床研究所涉及的治疗方法与药物包括瑞德西韦、间充质干细胞(MSCs)、洛匹那韦/利托那
韦、阿比朵尔、奥司他韦、达芦那韦/考比司他、糖皮质激素与中药。
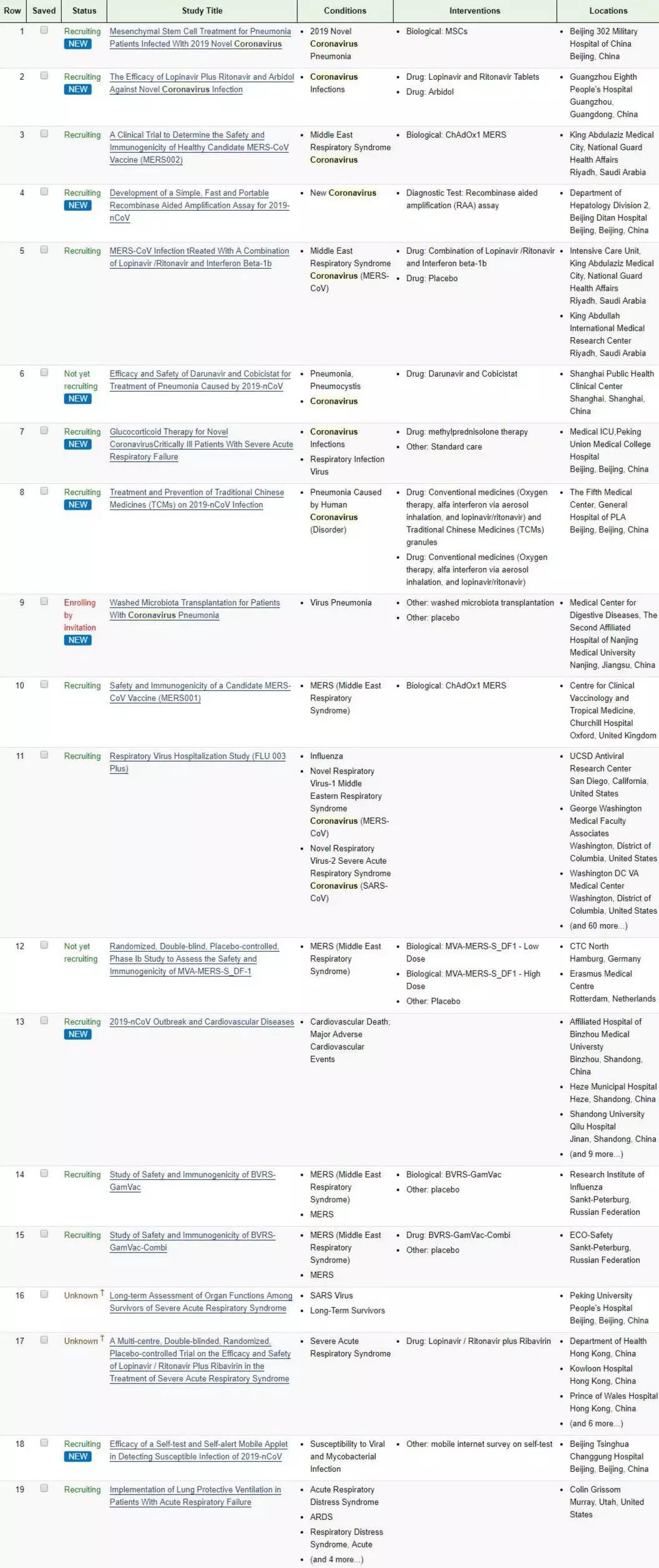
另外,根据科睿唯安统计显示,“目前全球冠状病毒活跃在研药物共有40多个,主要集中于MERS与SARS治疗,治疗用药物与疫苗各占一半”。根据
科睿唯安公布的全球处于活跃状态的冠状病毒治疗用药管线,所涉及治疗方法和药物包括血浆灌注、人单克隆抗体、干扰素、多肽、丝氨酸蛋白酶抑制剂、核蛋白抑
制剂和基因疗法等(点击查看:科睿唯安生命科学与制药微信公众号发布的“抗冠状病毒药物全球研发管线”情况)。
总结
从已获批药物来看,大部分抗病毒药物靶向病毒本身,难以在本次新型冠状病毒中发挥作用。少部分靶向宿主药物,虽然可能具有抗冠状病毒潜力,但由于上
市时间早,特异性不强且副作用较多。近年来随着抗病毒研究的不断深入,包括抗体药物和基因疗法在内的全新治疗方法均被用于研发之中,为抗病毒疗法创新提供
了新的可能。
然而由于药品特殊的经济学属性,过去获批上市的抗病毒药物主要是能带来收益的慢性感染药物和具有显著季节性特征的抗流感药物,而对于冠状病毒这类病
源不清,扩散及终止时间不明的急性病毒感染则缺少特异性治疗方法。近年来,随着技术发展与制药产业的快速变化,包括阿斯利康、赛诺菲、艾尔健、百时美施贵
宝在内的跨国制药巨头纷纷放弃抗生素及抗病毒领域的研究和开发工作,使得本就不热闹的抗病毒药物研发领域更显冷清。同样,虽然中国已经批准了许多抗病毒药
物,但在该领域自主研发中建树有限。
虽然此次新型冠状病毒疫情可能如2003年SARS类似在得到控制后平息,且不会再次发生。但针对相关病毒的研究、临床和药物研发不应该因为疫情的
结束而停止。在查询美国历年批准的抗病毒新药中,笔者注意到2018年FDA批准了首款天花特效药药物TPOXX,该药物后期研发由美国政府生物医学高级
研究与发展局资助,并在获批上市后购买200万份运输到国家战略储备。而对于已经经历两次冠状病毒疫情的我国,也应该由政府牵头并资助对冠状病毒进行长期
的科研及成果转化攻关。
 795532020/02/09 13:49
795532020/02/09 13:49



 发布文章
发布文章 APP下载
APP下载
















